Matériel
Pour réaliser un antibiogramme par la méthode des disques, il est nécessaire de disposer du matériel suivant :
- Une souche bactérienne en culture pure
- Un écouvillon stérile en coton
- Un tube à essai stérile de taille standard (Ø 16×160 mm – 18 mL)
- Géloses adaptées à la souche bactérienne : Mueller-Hinton, simple (MH) ou enrichie (MH-F)
- Un agitateur Vortex
- Un ensemenceur rotatif
- Un photomètre, ou à défaut les étalons 0,5 et/ou 1 de la gamme de McFarland
- Une feuille à fond strié
- Disques imprégnés du(des) antibiotique(s) testé(s)
- Un incubateur à 35°C
- Un décimètre ou un pied à coulisse
Étape 1 : Préparation de la souche bactérienne
La suspension bactérienne est préparée à partir d’une culture incubée 18 à 24h précédemment sur un milieu non-sélectif. Un écouvillon stérile en coton est utilisé pour prélever des colonies bactériennes de même morphologie, évitant la sélection d’un variant atypique. Les colonies sont ensuite émulsionnées dans une solution saline (NaCl 0,9%) et mélangées jusqu’à la turbidité requise (étalon 0,5 de la gamme MacFarland).
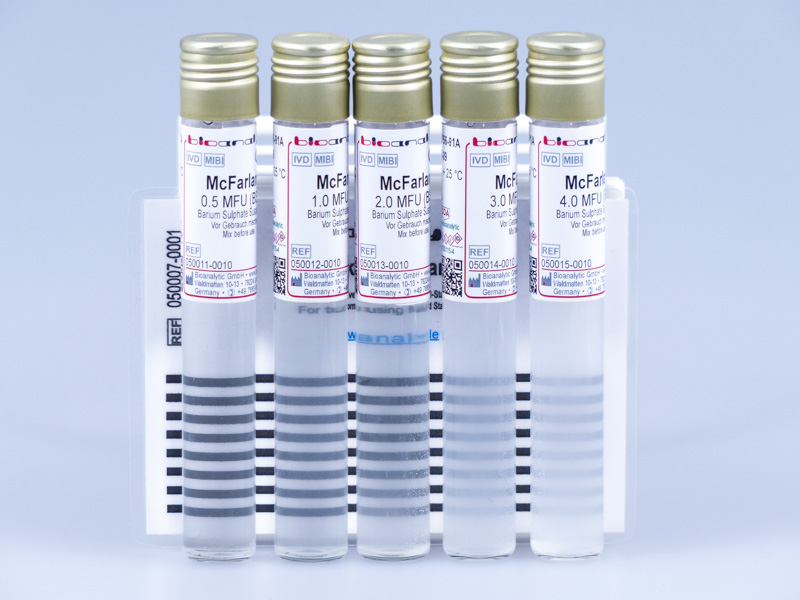
L’inoculum est utilisé idéalement dans les 15 minutes, et impérativement dans les 60 minutes suivant sa préparation.
Étape 2 : Choix de la gélose
Milieu standard Mueller-Hinton (MH)
- Enterobactéries,
- Pseudomonas spp,
- Enterococcus spp,
- Staphylococcus spp,
- Acinetobacter spp,
- Stenotrophomonas maltophili
Mueller-Hinton enrichi (MH-F)
- Streptocoques des groupes A, B, C et G,
- Streptococcuspneumoniae,
- Listeriamonocytogenes,
- Pasteurella multocida,
- Campylobacter jejuni et coli,
- Corynebacterium spp,
- Moraxella catarrhalis,
- Haemophilus influenzae,
- Streptocoques du groupe Viridans
Étape 3 : Inoculation de la gélose
L’ensemencement doit être réalisé sur des géloses ramenées à température ambiante et sèches. Si des gouttes d’eau sont visibles sur la gélose et/ou le couvercle de la boite, il est nécessaire de les sécher soit une nuit dans une pièce à 20-25°C, soit 15 min à 35°C. Les conditions d’asepsie doivent être assurées tout au long de la manipulation.
- Immerger l’écouvillon en coton stérile dans la suspension bactérienne (retirer l’excès de liquide en tamponnant l’écouvillon sur les bords internes du tube stérile)
- Ensemencer dans 3 directions différentes, décrit dans la figure suivante, ou bien à l’aide d’un ensemenceur rotatif.
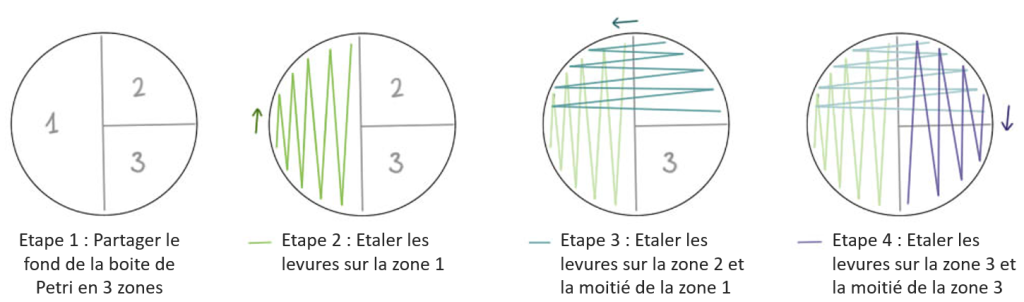
Étape 4 : Sélection des disques
Les recommandations de la CA-SFM établissent par espèce, ou groupe bactérien, deux listes d’antibiotiques à utiliser lors de la réalisation d’un antibiogramme.
La première de ces listes représente les antibiotiques à utiliser pour un antibiogramme dit « Standard ». Ces molécules dépendent du couple bactérie/molécule et correspondent aux antibiotiques naturellement efficaces contre la souche bactérienne, et ce, d’après les mécanismes de résistance naturelle de cette espèce bactérienne. Cette liste comprend aussi des antibiotiques à spectre large et des antibiotiques à spectre étroit ayant la souche bactérienne dans leur spectre. La seconde liste représente des antibiotiques dits « Complémentaires ». Ceux-ci ont un intérêt épidémiologique, notamment celui de détecter des mécanismes de résistance. D’autres antibiotiques sont qualifiés « d’Equivalent ». En effet, ces molécules permettent de représenter tout un groupe d’antibiotiques.
Ces antibiotiques sont qualifiés de « Antibiotiques Marqueurs », ils permettent la détection de mécanismes de résistance plus ou moins marqués, car ce sont des molécules, qui, au sein d’un groupe d’antibiotiques, sont les plus affines pour ces mécanismes, et permettent donc leur mise en évidence.
Veuillez trouver pour chaque espèce bactérienne les disques d’antibiotiques de choix dans les recommandations de la CA-SFM sur le lien suivant : https://www.sfm-microbiologie.org/2021/04/23/casfm-avril-2021-v1-0/
Étape 5 : Dépôt des disques et intubation
Il est recommandé de laisser les disques atteindre la température ambiante de la pièce. Le dépôt des disques se fait à la main à l’aide d’une pince, ou bien grâce à un distributeur automatique de disques. Les disques doivent être en contact ferme avec la gélose et ne doivent pas être déplacés par la suite.
Il est important de limiter le nombre de disques présents sur une gélose, il est recommandé de disposer :
- 6 disques : boîte de 90mm de diamètre,
- 12 disques : boîte de 150 mm de diamètre
- 16 disques : pour une boîte 120mm x 120mm
De manière générale, les disposer à une distance de 60 mm les uns des autres.
Attention ! Les disques d’érythromycine et de clindamycine doivent être placés à une distance de 12-20 mm bord à bord afin de détecter la résistance inductible aux lincosamides chez les Staphylocoques et les Streptocoques.
La mise en incubation doit se faire dans les 15 minutes suivant le dépôt des disques sur la gélose sans dépasser les 60 minutes. Pour les bactéries les plus courantes, il est nécessaire d’incuber les boîtes comme indiqué dans le tableau ci-dessous.
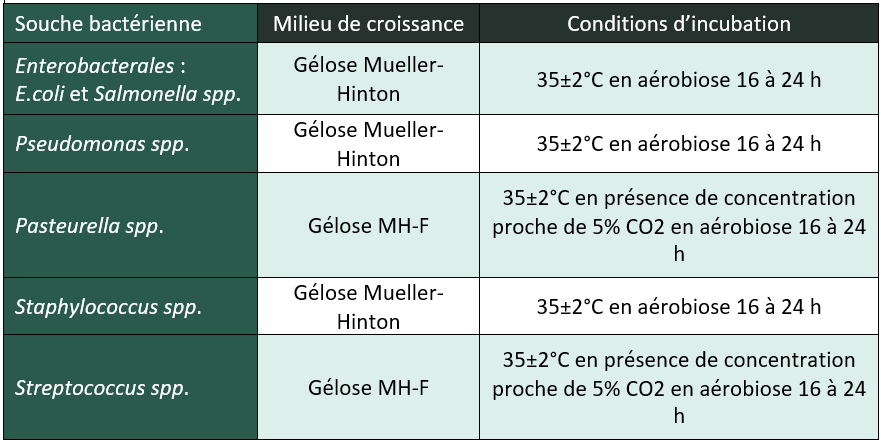
BRAVO ! L’antibiogramme est maintenant prêt à être lu !
Pour la suite de la démarche, il suffit de lire l’article DIY : Lire un antibiogramme.
