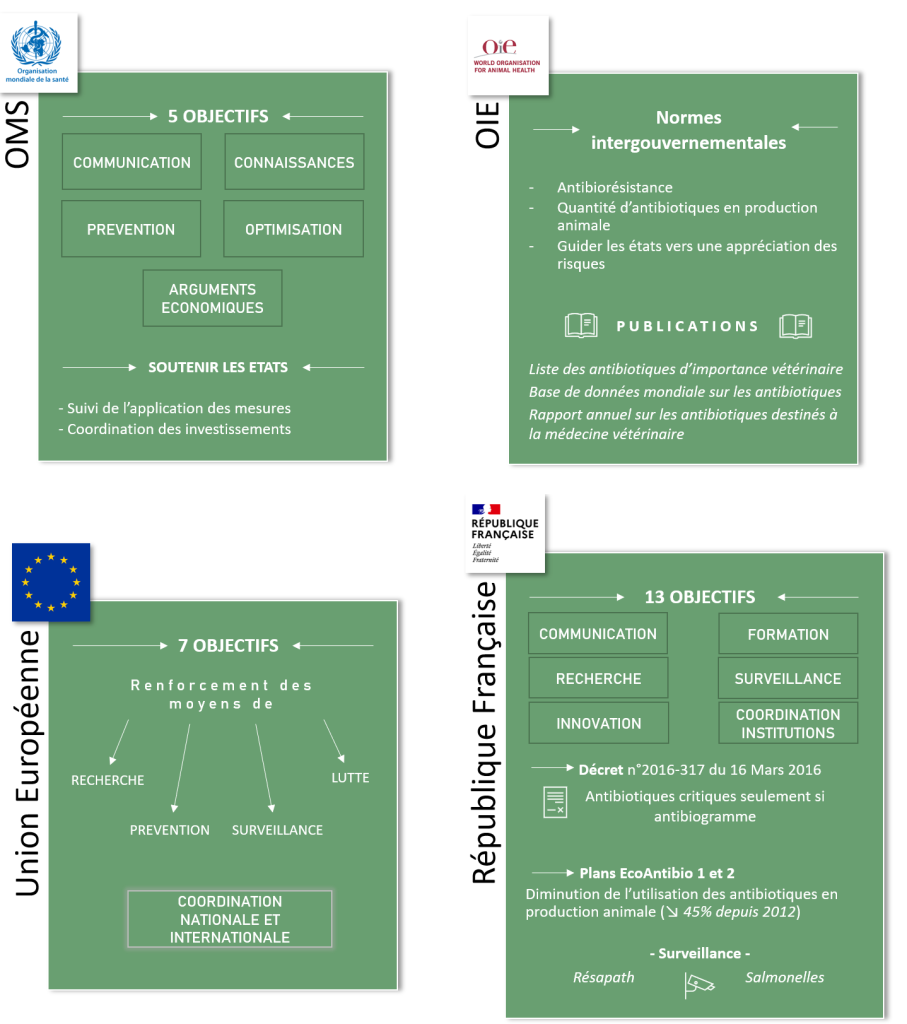
En France, la législation encadrant l’utilisation de l’antibiogramme est intrinsèquement liée à celle des antibiotiques dits « critiques ». En effet, la règlementation a été établie par le décret n° 2016-317 du 16 mars 2016, paru au Journal Officiel de la République Française le 18 mars 2016 et entré en vigueur le 1er avril 2016. Ce décret établi un cadre « relatif à la prescription et à la délivrance des médicaments utilisés en médecine vétérinaire contenant une ou plusieurs substances antibiotiques d’importance critique », il concerne à la fois « vétérinaires ; pharmaciens d’officine ; fabricants d’aliments médicamenteux ; laboratoires d’analyses biologiques ».
Les substances antibiotiques d’importance critique sont définies par une liste de substances actives, par les articles L.5144-1-1 et R.5141-117-2 de l’arrêté du 18 mars 2016. Ces substances sont définies comme des « substances antibiotiques d’importance critique (…) dont l’utilisation doit être prioritairement préservée dans l’intérêt de la santé humaine et animale ».
Antibiotiques critiques en médecine vétérinaire
- Céphalosporines de 3ème génération :
- Céfopérazone, Céftiofur, Céfovécine
- Céphalosporine de 4ème génération :
- Céfquinome
- Fluoroquinolones :
- Danofloxacine, Enrofloxacine, Marbofloxacine, Orbifoxacine et Pradofloxacine
Ainsi, ces antibiotiques ne doivent pas être utilisés en première intention sauf en absence d’une autre molécule efficace pour la prise en charge thérapeutique de l’infection bactérienne. Cependant, leur prescription doit être subordonnée « à la réalisation préalable d’un examen clinique », « à la réalisation préalable d’un examen complémentaire visant à identifier la souche bactérienne » et « à la réalisation préalable d’un examen complémentaire visant à démontrer la sensibilité de la souche bactérienne identifiée à cet antibiotique au moyen d’un test de sensibilité réalisé selon une des méthodes fixées par arrêté conjoint des ministres chargés de la santé et de l’agriculture » selon les articles L.5144-1-1 et R.5141-117-2 de l’arrêté du 18 mars 2016
Et en cas d’urgence ?
Néanmoins, en cas d’urgence (septicémie, choc toxique…), ceux-ci peuvent être prescrit en 1ère intention selon le contexte clinique et épidémiologique, « lorsqu’il s’agit d’un cas aigu d’infection bactérienne pour laquelle un traitement avec d’autres familles d’antibiotiques serait insuffisamment efficace ». En parallèle, il a l’obligation de réaliser un antibiogramme. Toutefois, « dans un délai de quatre jours après la prescription, le vétérinaire adapte le traitement en fonction de l’évolution du contexte clinique et épidémiologique et des résultats des examens complémentaires portés à sa connaissance. »
Ainsi, en fonction des résultats d’analyses et de l’évolution clinique, l’antibiothérapie devra être adaptée. Les résultats de l’antibiogramme sont valables 3 mois pour la même affection du même animal ou animal du même site, avec une ordonnance valable 1 mois. Après ce délai, et en vue d’une prolongation du traitement, un examen clinique devra être fait. Les résultats de l’antibiogramme doivent être conservés pendant une durée de 5 ans.
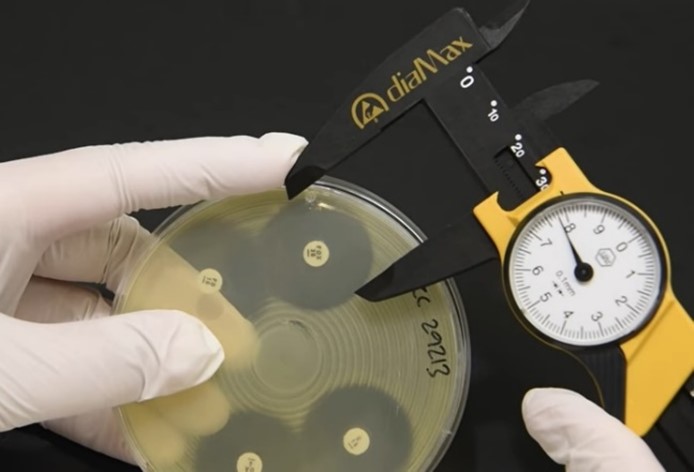
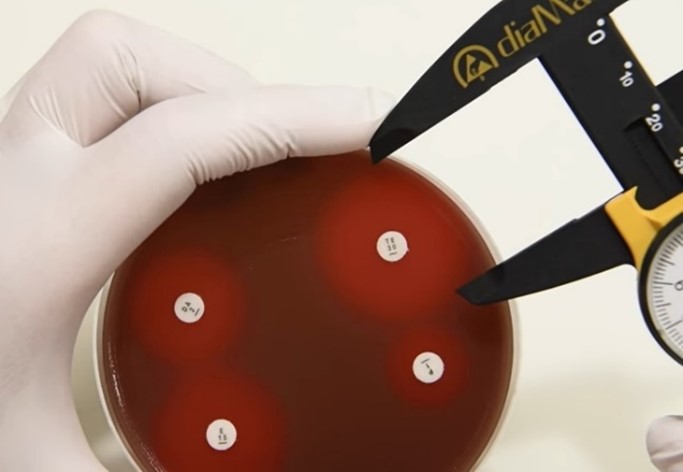
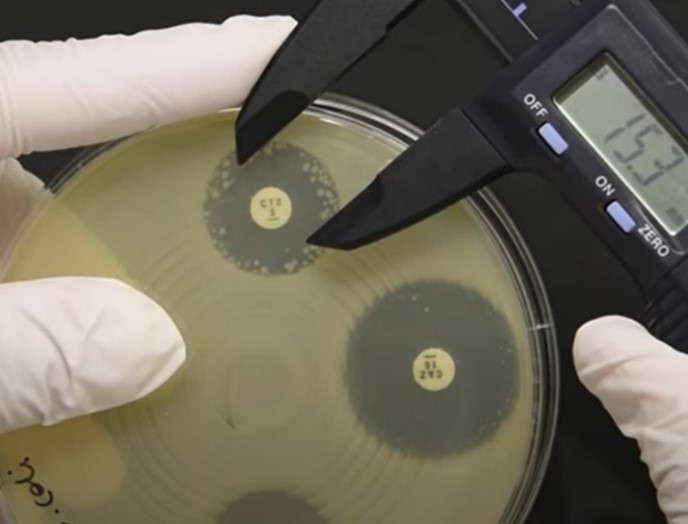
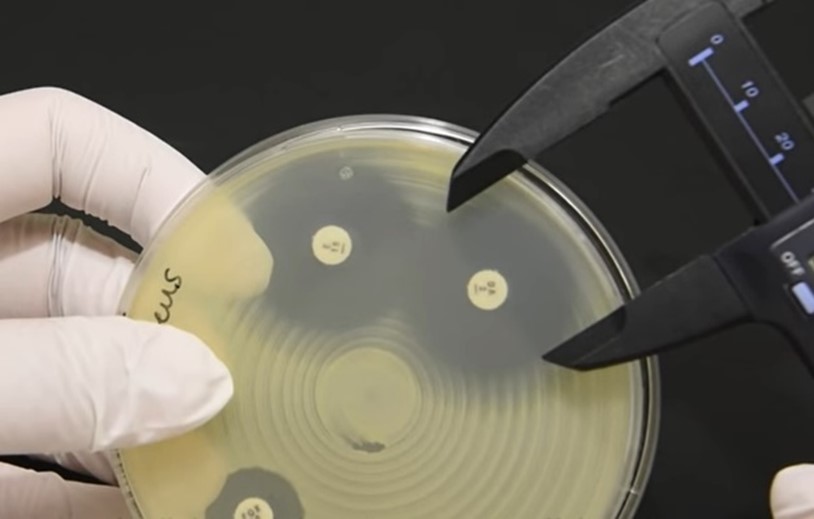
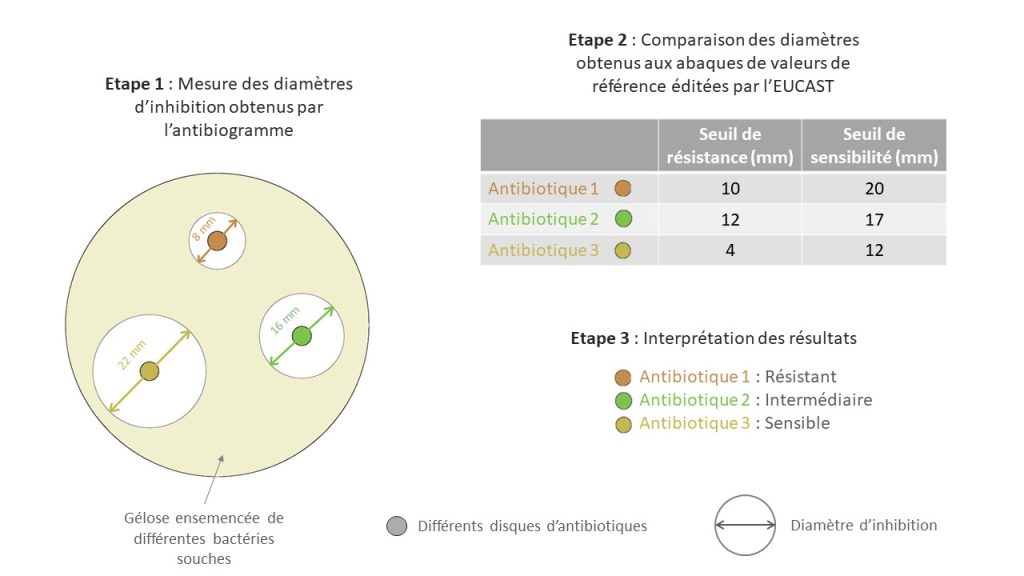
Pour justifier la prescription d’un antibiotique critique, seul l’antibiogramme réalisé par la méthode des « disques » selon les normes NF U47-106 et NF U47-107 et la méthode de dilution en milieu liquide sont recevables par la réglementation, y compris pour les antibiogrammes réalisés en clinique vétérinaire par le praticien !